Hidrokarburet
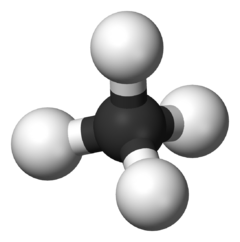
Hidrokarburet janë substanca të cilat bëjnë pjesë në grupin e kimisë organike , dhe janë të përbëra prej dy elementësh kryesorë karbonit dhe hidrogjenit. Hidrokarburet janë burime të rëndësishme në ushqimin e njeriut si përbërje e frutave , karotës ,në përbërjen e vajit të bimëve të larta, po ashtu gjenden edhe në përbërjen e naftës, gazi nëntokësor. Hidrokarburet janë të ndara në hidrokarbure aciklike dhe hidrokarbure ciklike.
Hidrokarburet Aciklike[Redakto | Redakto nëpërmjet kodit]
Hidrokarburet aciklike ndryshe quhen alimfatike dhe janë të ndara në dy grupe: Hidrokarbure të ngopura dhe hidrokarbure të pangopura.
- Hidrokarburet e ngopura ndryshe quhen Alkane dhe kanë karakteristikë lidhjen njëfishe ( C-C ) të cilat gjatë emërtimit marrin prapashtesën -AN dhe kanë formulë të përgjithshme CnH2n+2.
- Hidrokarburet e pangopura ndahen në Alkene dhe Alkine. Alkenet si karakteristikë kanë lidhjen dyfishe ( C=C ) dhe gjatë emërtimit marrin papashtesën -EN dhe kanë formulë të përgjithshme CnH2n. Alkinet kanë karakteristikë lidhjen trefishe ( C≡C ) gjatë emërtimit marrin prapashtesën -IN kanë formulë të përgjithshme CnH2n-2.
Hidrokarburet Ciklike[Redakto | Redakto nëpërmjet kodit]
Hidrokarburet Ciklike ndryshe quhen aromatike ndahen në dy grupe: Cikloalkan dhe Cikloalken
- Cikloalkanet emërtohen nëse emrit të alkanit i shtohet parashtesa CIKLO d.m.th. Ciklo+Alkan=Cikloalkan psh. ( ciklopropan C3H6 ) dhe kanë formulë të përgjithshme CnH2n ku n≥3.
- Cikloalkenët emërtohen nëse emrit të alkenit i shtohet parashtesa CIKLO d.m.th. Ciklo+Alken=Cikloalken psh. ( ciklopenten C5H8 ) dhe kanë formulë të përgjithshme CnH2n-2 ku n≥3.
Vetitë[Redakto | Redakto nëpërmjet kodit]
Shembuj të hidrokarbureve dhe variacioneve të tyre[Redakto | Redakto nëpërmjet kodit]
Përftimi[Redakto | Redakto nëpërmjet kodit]
a)Përftimi i alkaneve me anë të sintezës së Vurcit
b)Gatitja e alkaneve në laborator
Përdorimi[Redakto | Redakto nëpërmjet kodit]
Hidrokarburet janë një nga burimet më të rëndësishme energjitike të tokës. Janë mbizotërues të përdorimit të hidrokarbureve është si një burim i djegshëm i karburantit. Në formën e tyre të ngurtë, hidrokarburet marrin formën e asfaltit. Metani dhe etani janë në gjëndje të gaztë në temperaturat normale dhe nuk mund të jetë i lëngshëm nga presioni i vetëm. Propani është megjithatë lëng i lehtë, dhe ekziston më së shumti si një lëng. Butan është lëng i lehtë. Pentani është i lëngshëm në temperaturën normale, që zakonisht përdoret në kimi dhe industri si një lëndë gati pa erë të fuqishme. Heksani është gjithashtu është një jo-polar, jo-aromatik, tretës, si dhe një pjesë e rëndësishme e zakonshme benzinë. Heksani dhe oktanit - alkanët, alkenët dhe cikloalkanët izomerik janë komponentët kryesorë të benzinës, naftës, dhe përzierje tretës industriale.
Djegia e karburantëve[Redakto | Redakto nëpërmjet kodit]
Hidrokarburet aktualisht janë burimi kryesor i botës së energjisë elektrike dhe ngrohjes burimeve (si për shembull në shtëpi për ngrohje) për shkak të energjisë së prodhuar duke djegur. Shpesh kjo energji është përdorur si drejtpërdrejt në ngrohjen si ngrohës në shtëpi, të cilat i përdorin ose të naftës apo gazit natyror. Diegia e hidrokarbureve është përdorur për të ngrohur ujë, e cila pastaj është qarkulluar. Një parim i ngjashëm është përdorur për të krijuar energji elektrike në termocentralet. Metani lironvetëm një dioksid karboni (CO2) për dy Molekulat e ujit ( H2O ).
Veti karakteristike të hidrokarbureve janë që ata prodhojnë avull, dioksid karboni dhe nxehtësi gjatë djegies dhe se duhet oksigjen që djegia të ndodhë. Hidrokarburi më i thjeshtë, metani, digjet kështu:
- CH4 + 2 O2 → 2 H2O + CO2 + Energji
Një tjetër shembull është propani:
- C3H8 + 5 O2 → 4 H2O + 3 CO2 + Energji
Djegia e hidrokarbureve është një shembull i një reaksioni kimik ekzotermik.

