Aminoacidet

Aminoacidet janë njësi themelore të molekulave proteinike. Në ndërtimin e këtyre të fundit marrin pjesë 20 lloje të aminoacideve. Të gjitha aminoacidet që marrin pjesë në ndërimin e molekulave proteinike janë të formës L.
Aminoacidet janë përbërje organike me peshë të vogël molekulare, të cilat në molekulën e tyre kanë së paku një grup karboksil () dhe një grup amin (). Prandaj, mund të thuhet se këto janë acide organike, në molekulën e të cilave gjëndet së paku një grup amin. Të gjitha aminoacidet përmbajnë C, H, O, dhe N, përveç këtyre elementeve kimike përmbajnë edhe S. Formula molekulare e aminoacideve është:
R- e zëvëndëson mbetjen e aminoacideve që hyjnë në ndërtim të proteinave. Grupi anësor R është i lirë në vargje peptidike dhe ai e përcakton formën e proteinës në hapërsirë, funksionin dhe aktivitetin e saj biologjik.
Dallohen dy forma sterike të aminoacideve: forma L dhe forma D. Aminoacidet që i takojnë formës L gjenden në proteina. Grupi amin, (), është i lidhur me atomin e karbonit, i cili gjendet afër grupit karboksil. Këto aminoacide quhen a-aminoacide. Atomi i karbonit, me të cilin është i lidhur grupi amin, është asimetrik, që do të thotë se aminoacidet janë përbërje optikisht aktive, përveç aminoacidit më të thjeshtë – glicinës. Pra, kur aminoacidet gjenden në tretësirë, ato e kthejnë rrafshin e dritës së polarizuar.
Meqënëse aminoacidet kanë një grup karbosil dhe një grup amin, ato veprojnë si acide dhe si baza, që do të thotë se kanë karakter amfotern.
Klasifikimi i aminoacideve
[Redakto | Redakto nëpërmjet kodit]Peptidet krijohen me lidhjen e një numri të vogël të aminoacideve në mes veti. Prandaj peptidet pas dukurisë së hidrolizës na japin aminoacidet, apo aminoacidet lidhen në mes veti duke na dhënë lidhje peptidike.
Aminoacidet janë bazë e krijimit të lidhjeve peptide, dipeptide, dhe tri e polipeptidikee. Edhe proteinat të cilat në strukturën e tyre janë pjesë përbërse e substancave kryesore organike me të cilat është e ndërtuar organizmi, janë të përbëra prej aminacideve, edhe atë mundë të themi se proteinat janë të përbëra prej më tepër se njëqind aminoacideve në ndërtimin e molekulës së tyre.
Me rritjen e vargut të polipeptideve, të përbërë prej më tepër se 100 aminoacideve, krijohen molekulat e proteinës, e cila thamë se është kushti kryesor i mbajtjes gjallë të organizmit. Funksioni i molekulës së peptideve varet nga numri i llojit të aminoacideve dhe renditjes së tyre në varg.
Emërtimi i aminoacideve që janë të lidhura në varg bëhet në atë mënyrë që aminoacidi i cili futet në reaksion me grupin karboksil e merr parashtesën il , kurse emri i aminoacidit që nuk futet në reaksion me grupin karboksil, nuk ndryshon fare. Psh glutationi është një tripeptid i cili është i izoluar prej disa organeve dhe gjendet edhe në gjak.Ky ka një rol të rëndësishëm në organizëm duke marrë pjesë në të gjitha proceset oksido reduktuese, si transportues i hidrogjenit në organizëm. Ekzistojnë 20 lloje aminoacidesh, të cilat marrin pjesë në strukturën e proteinave. Mund të bëhet klasifikimi kimik dhe biologjik i aminoacideve.
Klasifikimi kimik
[Redakto | Redakto nëpërmjet kodit]Në bazë të strukturës kimike aminoacidet ndahen në tri grupe:
- Aminoacide alifatike (aciklike)
- Aminoacide aromatike
- Aminoacide heterociklike.
Disa aminoacie alifatike kanë në molekulën e vet një grup amin dhe një grup karboksil (aminoacidet monoaminomonokarboksilike), p.sh.glicina, alanina, valinaetj. Disa të tjera përmbajnë një grup amin e dy grupe karboksile (aminoacidet monoamindikarboksilike), p.sh. acidi asparik, acidi glutaminik etj., kurse disa aminoacide të tjera të këtij grupi përmbajnë në molekulën e tyre grup –OH p.sh serina dhe troina, kurse cisteina, cistina dhe metoina përmbajnë në molekulën e vet sulfur.
Kur është fjala për aminoacide ciklike, dallohen dy grupe: aminoacide izocilike, të cilat në molekulën e tyre përmbajnë unazën e benzolit (fenil- alanina dhe tirozina) dhe aminoacide heterociklike, të cilat në molekulën e vet përmbajnë azot ose ndonjë element tjetër (triptofani, histidina, prolina dhe hidoksiprolina). Aminoacide alifatike (aciklike-jorrethore)
Disa aminoacide alifatike kanë një grup amin dhe një grup karboksil, të ashtuquajturat aminoaide monoaminokarboksilike, si psh.glicina, alanina, valina, etj. Disa aminoacide përmbajnë një grup amin e dy grupe karboksile- aminoaidet monoaminokarboksilike, si psh. acidi asparaginik, glutaminik, etj. Kurse disa aminoacide tjera prej këtij grupi përmbajnë në molekulën e vet dy grupe amine dhe një grup karboksil, aminoacidet diaminomonokarboksilike, siç janë psh. lizina, arginina etj. Disa aminoacide alifatike përmbajnë në molekulën e vet grupën –OH, si psh: serina dhe treonina, kurse cisterina, cistina dhe metionina, përmbajnë në molekulën e vet sulfur S.
Aminoacide aromatike (ciklike-rrethore)
[Redakto | Redakto nëpërmjet kodit]Ky lloj i aminoacideve mundë të ndahet në dy nëngrupe: a) Aminoacide izociklike dhe në b) Aminoacide heterociklike Të parat në molekulën e vet përmbajnë unazën e benzolit, fenil-alanina,tirozina, etj, dhe të dytat, aminoacidet heterociklike në molekulën e vet përmbajnë unazën heterociklike, që do të thotë se në unazë përveq karbonit këto aminoacide përmbajnë edhe azot ose ndonjë element tjetër, siç është triptofani, histidina etj.
Aminoacidet aromatike
[Redakto | Redakto nëpërmjet kodit]Klasifikimi aromatik i aminoacideve. – Organizmi i njeriut është i aftë që disa aminoacide t’i sintetizojë vet, kurse disa aminoacide që nuk mund t’i sintetizojë duhet t’i marrë përmes ushqimit, sepse janë të domosdoshme për jetë. Ato aminoacide që mund t’i sintetizoj organizmi i njeriut quhen aminoacide joesenciale (apo aminoacide të zëvendësueshme), kurse aminoacidet që nuk mund t’i sintetizoj organizmi i njeriut quhen aminoacide esenciale (aminoacide të pa zëvendësueshme)
Klasikimi biologjik
[Redakto | Redakto nëpërmjet kodit]Organizmi i njeriut është i aftë që disa aminoacide vetë t’i sintetzojë, kurse disa aminoacide, që nuk mund t’i sintetzojë, duhet t’i marrë përmes ushqimit, sepse janë të domosdoshme për jetë. Aminoacidet që mund t’i sintetizojë organizmi i njeriut quhen aminoacide joesenciale (aminoacide të zëvëndësushme), kurse aminoacidet që nuk mund ti sintetizojë quhen aminoacide esenciale (aminoacide të pazëvëndësueeshme). Aminoacidet janë komponime organike me peshë të vogël molekulare, të cilat në molekulën e tyre kanë së paku një lidhje karboksile (), dhe një grup amin (). Prandaj mund thuhet se aminoacidet janë komponime organike, apo acide organike në molekulën e të cilave gjendet më së paku një grup amin. Të gjitha aminoacidet përmbajnë C,O,H dhe N, e disa prej tyre përveç këtyre elementeve kimike përmbajnë edhe S.
Grupi amin() te numri më i madh i aminoacideve është i lidhur për atomin e karbonit, i cili gjendet afër grupit karboksil, gjegjësisht për alfa atomin e karbonit.Këto aminoacide quhen alfa aminoacide. Atomi i karbonit për të cilin është i lidhur grupi amin është asimetrik, çka do të thot se aminoacidet janë komponime aktivisht aktive, përveq komponimit acidik më të thjeshtë- glicinës.Pra kur aminoacidet gjenden në tretësirë ato e kthejnë rrafshin e dritës së polarizuar, kjo është vërtetuar në mënyrë eksperimentale. Me qenëse aminoacidet kanë më së paku një grup karboksil () dhe një grup amin () ato veprojnë si acide por edhe si baza, që do të thotë se kanë një karakter amfotern (amfolit).
Vetitë e aminoacideve
[Redakto | Redakto nëpërmjet kodit]Aminoacidet kanë veti të ndryshme fiziko- kimike: aktiviteti optik, amfoteriteti, pjesëmarrja në reaksionet e ndryshme biokimike, krijimi i lidhjes peptidike etj. Aktiviteti optik- Aminoacidet janë komponime optikisht aktive (përveç aminoacidit më të thjeshtë- glicinës), sepse të gjitha përmbajnë atom asimetrik të karbonit. Pra, ato e kthejnë rrafshin e dritës së polarizuar. Atomi i karbonit, për të cilin është i lidhur grupi amin, është asimetrik
Amforteriteti i aminoacideve
[Redakto | Redakto nëpërmjet kodit]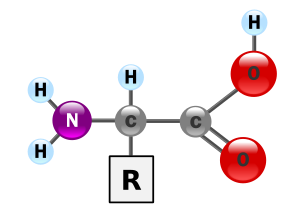
Meqë aminoacidet në molekulën e tyre kanë grup karboksil () dhe grupin aminik (-NH), ato kanë veti të acideve dhe të bazave. Kjo tregon se aminoacidet bëjnë pjesë në grupin e komponimeve amfotere (amfolite). Aminoacidet në tretësirë gjenden si jone dypolëshe, të cilat quhen zviterion (amifon). Duke marrë parasysh se zmmz aminoacidet disosohen dobët, atëherë në disosimin e tyre ndikojnë acidet dhe bazat të tjera.
Nëse tretësirës së aminoacideve i shtohet ndonjë bazë e fortë, atëherë pengohet disosimi bazik i aminoacidit dhe shprehet disosimi bazik i aminoacidit dhe shprehet disosimi i grupit karboksil. Në këtë rast aminoacidi do të ketë veti të acidit të dobët dhe me shtimin e bazës jep krypë. Nëse shtohet acidi, atëherë pengohet disosimi i grupit karboksil, për ç’arsye disosohen si baza grupet amine të aminoacidit dhe me acid japin kripë. Nëse i shtohet formaldehidi tretësirës së aminoacidit, atëherë shkaktohet bllokimi i grupit amin, për ç’arsye aminoacidi disosohet si acid. Nëse bëhet titrimi me bazë (NaOH), atëherë mund të përcakëtohet edhe numri i grupeve të lira karboksilike të aminoacideve.
Ndikimi i acidit nitror- Acidi nitror e oksidon grupin amin dhe prej tij e liron azotin. Në këtë mënyrë prej sasisë së liruar të azotit mund të përcakëtohet edhe numri i molekulave të aminoacideve në ndonjë përzierje. Aminoacidet reagojnë reagojnë me CO2 në inde dhe japin komponime karbamine. Në këtë parim hemoglobina e lidh CO2 në inde dhe e çon deri në mushkëri.
VETITË E AMINOACIDEVE
Aminoacidet kanë veti të ndryshme fiziko-kimike: aktiviteti optik, amfoteriteti, pjesëmarrja në reaksionet e ndryshme biokimike, krijimi i lidhjes peptidike etj. Aktiviteti optik. – Aminoacidet janë komponime optikisht aktive (përveç aminoacidit më të thjeshtë glicinës) sepse të gjitha përmbajnë atom asimetrik të karbonit. Pra, ato e kthejnë rrafshin e dritës së polarizuar. Amfoteriteti i aminoacideve. – Meqenëse aminoacidet në molekulën e vet kanë një grup karboksil (COOH) dhe grupin amin (- NH2 ) ato kanë veti të acideve dhe bazave. Kjo na tregon se aminoacidet bëjnë pjesë në grupin e komponimeve amfotere (amfolite).
Veçoritë kryesore të Aminoacideve
Aminoacidet faktikisht janë komponime organike me një peshë shumë të vogël molekulare të cilat në molekulën e tyre kanë së paku një grup karboksil (COOH) dhe një grup amin (NH2). Prandaj thuhet se këto komponime organike janë acide organike ku mbrenda molekulës së tyre gjendet së paku një grup amin ().
Shkencëtari amerikan i biokimisë Marshall Niremberg, në vitin 1968 fitoi çmimin Nobel në fiziologji – medicinë për kontributin e çmueshëm që dha në hulumtimin e pavarur që bëri mbrenda të ashtuquajturit “kod gjenetik” duke treguar se si kombinimet e ndryshme të bazave mbrenda aminoacideve përgatisin qelizën të formojë proteina.
Lajmëtari gjenetik (ARN) apo kodi gjenetik i tillë është një mostër ose model për sintezën e proteinave. Ky lajmëtar përbëhet nga një seri e nukleotideve ku secila prej tyre përmban njërin prej katër bazave nitrogjene: urucilin, citozinën, adeninën dhe guaninën. Aminoacidet janë një klasë shumë e rëndësishme e komponimeve organike të cilat përmbajnë grupin amin (NH2) dhe grupin karboksil (COOH). Pasi që aminoacidet janë bartës kryesorë të kodit gjenetik për zintezën e proteinave,apo na japin njësinë strukturore të tyre, atëherë 20 më kryesoret prej të gjitha llojeve të aminoacideve shërbejnë si tulla ndërtimore të proteinave (shih proteinat).
Këto aminoacide janë të njohura si standarde ose alfa (a) aminoacide dhe në këtë grup janë të përfshira: Alaninet, Argininet, Asparaginet, acidi aspartik, cisteinet, acidi glutamik, glutaminet, glucinet, histidinet, leucinet, lysinet, metionimet, fenylaninet, pralinet, serinet, threaninet, tryptofaninet, tyrosinet dhe valinet. Është e njohur se proteinat janë përbërësit kryesorë i të gjitha gjallesave. Me dukurinë e hidrolizës, proteinat shëndrrohen në aminoacide, dhe në organizëm këto dy komponime organike janë të lidhura ngushtë njëra me tjetrën. Pra, metabolizmi i aminoacideve është i ndërtuar bashkarisht me metabolizmin e proteinave. Organizmi i njeriut dhe i shumicës së shtazëve nuk mundet vetvetiu të ndërtijë të gjitha aminoacidet. Disa lloje të aminoacideve merren përmes ushqimit, kështu që disa lloje të aminoacideve i veçojmë si komponime organike tepër të nevojshme dhe esenciale për organizmin.
P.sh. disa lloje të aminoacideve si: arginini, prolini, serini, tirozini dhe cistini ndikojnë në rritjen e njeriut, pra formojnë trupin e tij. Këto aminoacide i krijon vetë organizmi, por si duket jo në masë të mjaftueshme për çka duhet të merren me ushqim nëse duam zhvillim normal (p.sh. të fëmijëve tanë).
Krijimi i lidhjes peptidike
[Redakto | Redakto nëpërmjet kodit]Kjo është vetia më e rëndësishme biokimike e aminoacideve, sepse mundëson lidhjen e aminoacideve midis vete, me ç’rast një aminoacid reagon në grupin amin të aminoacidit tjetër, me ç’rast krijohet lidhja peptidike. Komponimi që krijohet me lidhjen e dy aminoacideve quhet dipeptid, me lidhjen e tri aminoacideve të njëjta ose të ndryshme krijohet tripeptidi e kështu me rashë. Me lidhjen e shumë peptideve krijohet komponimi që dë të jetë oligopeptid ose molekulë proteinike, që varet nga numri i aminoacideve. Në oligopeptide bëjnë pjesë molekulat e ndërtuara prej 2-10 aminoacidesh, në polipeptide ato të ndëruara prej 10-100 aminoacidesh, në proteina ato të ndërtuara prej më shumë se 100 aminoacidesh. lidhja me e forte tek aminoacidet. bashkimi i disa aminoacideve na formon Cili nga ciftet e aminoacideve te ka ngarkese negative te readikalit ne pH 8.0 a. Asparagine & Glutamine b. Leucine & Glycina c. Histidine & Lysine d. Aspartate & Glutamate



