Alkanet
Alkanet, të njohur si vajra, janë përbërjet kimike që përbëhen vetëm prej elementeve të karbonit C dhe hidrogjenit H ( p.sh.: hidrokarburet), ku këto atome janë të lidhur së bashku me vetem një lidhje kovalente (do të thotë, ato janë përbërje të ngopura) aciklike (do të thotë jounazore).
Çdo atom i karbonit duhet të ketë 4 lidhje qoftë C-H (do të thotë, të lidhet me atome të hidrogjenit) apo lidhje C-C (do të thotë lidhje me atome tjera siç është karboni, pra te jetë i lidhur me katër atome të tjera) dhe çdo atom i hidrogjenit duhet të jetë i lidhur me një atom të karbonit.
Një varg i atomeve të karbonit është i njohur si strukturë karbonike. Në përgjithësi, numri i atomeve të karbonit përdoren shpesh për të përcaktuar përmasat e alkanëve (p.sh.: C2 - alkane).
Hidrokarburet e ngopura kanë formulë të përgjithshme CnH2n+2 kurse për radikalët CnH2n+1 ku atomet të karbonit janë bashkuar në një strukturë. Hidrokarburet e ngopura janë të ndarë në alkane dhe cikloalkane, ato nuk kanë struktura të ngjashme dhe në kuptim të gjerë cikloalkanet nuk janë alkane. Megjithatë, ndonjëherë cikloalkanet janë quajtur alkane ciklike, emërtim i cili mund të jetë konfuz, sepse në të vërtetë alkanet quhen alkane aciklike.
Përfaqesuesi kryesor i alkaneve, është metani me formulë molekulare CH4. Nuk ka asnjë kufizim për numrin e atomeve të karbonit që mund të jenë të lidhura së bashku, i vetmi kufizim: është molekulë ciklike, e ngopur dhe është një hidrokarbur. Hidrokarburet e ngopura dhe vajrat më të rëndë janë shembuj të alkaneve ku numri i atomeve të karbonit mund të jetë më i madh se 10.
Alkanët nuk janë shumë reaktive dhe kanë pak aktivitet biologjik.
Izomeria
[Redakto | Redakto nëpërmjet kodit]Izomeria e alkaneve dhe hidrokarburëve në përgjithësi ka të bëjë me strukturë dhe veti (kimike e fizike) të ndryshme në krahasim me alkanin përkatës. Alkanet me një numër karbonesh më të madh se tre mund të organizohen dhe renditen në mënyra të ndryshme duke dhënë kështu izomere strukturorë. Izomeri më i thjeshtë për alkanet është ai në të cilin të gjitha atomet e karbonit vendosen në një varg të vetëm pa degëzime. Këta izomerë quhen 'normal' (n-pentan, n-eptan) sipas sistemit IUPAC. Numri i izomerëve rritet në mënyrë të shpejtë me rritjen e numrit të atomeve të karbonit.
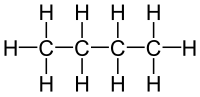  |
| Figura : Ndryshimi i strukturës së butanit. |
Emërtimi-Nomenklatura
[Redakto | Redakto nëpërmjet kodit]Emërtimi bëhet në bazë të numrave greko-latinë duke u shtuar prapashtesën AN për alkanet dhe IL për alkanët radikalë.
| Nr | Emri greko-latin | Alkanët | n = | Formula CnH2n + 2 | Radikalët e Alkanëve | n = | Formula CnH2n + 1 |
|---|---|---|---|---|---|---|---|
| 1 | Meta | Metan | n = 1 | CH4 | Metil - Radikal | n = 1 | CH3 |
| 2 | Eta | Etan | n = 2 | C2H6 | Etil - Radikal | n = 2 | C2H5 |
| 3 | Propa | Propan | n = 3 | C3H8 | Propil - Radikal | n = 3 | C3H7 |
| 4 | Buta | Butan | n = 4 | C4H10 | Butil - Radikal | n = 4 | C4H9 |
| 4 | Penta | Pentan | n = 5 | C5H12 | Pentil - Radikal | n = 5 | C5H11 |
| 6 | Heksa | Heksan | n = 6 | C6H14 | Heksil - Radikal | n = 6 | C6H13 |
| 7 | Hepta | Heptan | n = 7 | C7H16 | Heptil - Radikal | n = 7 | C7H15 |
| 8 | Okta | Oktan | n = 8 | C8H18 | Oktil - Radikal | n = 8 | C8H17 |
| 9 | Nona | Nonan | n = 9 | C9H20 | Nonil - Radikal | n = 9 | C9H19 |
| 10 | Deka | Dekan | n = 10 | C10H22 | Dekil - Radikal | n = 10 | C10H21 |
Dukuritë të alkanëve
[Redakto | Redakto nëpërmjet kodit]Dukuritë në univers
[Redakto | Redakto nëpërmjet kodit]Dukuritë në tokë
[Redakto | Redakto nëpërmjet kodit]Dukuritë biologjike
[Redakto | Redakto nëpërmjet kodit]Dukuritë ekologjike
[Redakto | Redakto nëpërmjet kodit]Produktet
[Redakto | Redakto nëpërmjet kodit]Përdorimi
[Redakto | Redakto nëpërmjet kodit]Alaknet kanë përdorim të gjerë në jetën e përditshme. Përdoren si lëndë të djegshme, për ndriçim dhe si lëndë të parë për industrinë kimike, farmaceutike, kozmetike, të masave plastike, si tretës etj.
Vetitë fizike
[Redakto | Redakto nëpërmjet kodit]Alkanet dhe cikloalkanet janë gaze dhe lëngje, me rritjen e masës molekulare të tyre temperatura e vlimit rritet. Hidrokarburet e ngopura nuk kanë grup funksionor, pra s'kanë ato apo grupime atomike të cilat do t'i përcaktojnë vetitë fizike e kimike të tyre. Ato janë substanca pak aktive dhe për këtë arsye janë quajtur në fillim parafina, e cila është marrë nga fjala latinisht parum affinis që do të thotë pak të afta.
| EMRI | Formula | B.P./oC | M.P./oC | Dendësia/g cm −3(20oC) |
| Metan | CH4 | -162 | -183 | gas |
| Etan | C2H6 | -89 | -172 | gas |
| Propan | C3H8 | -42 | -188 | gas |
| Butan | C4H10 | -0.5 | -135 | gas |
| Pentan | C5H12 | 36 | -130 | 0.626 |
| Heksan | C6H14 | 69 | -95 | 0.659 |
| Heptan | C7H16 | 98 | -91 | 0.684 |
| Octan | C8H18 | 126 | -57 | 0.703 |
| Nonan | C9H20 | 151 | -54 | 0.718 |
| Decan | C10H22 | 174 | -30 | 0.730 |
| Undecane | C11H24 | 196 | -26 | 0.740 |
| Dodecane | C12H26 | 216 | -10 | 0.749 |
| Triacontane | C30H62 | 343 | 37 | solid |
Vetitë kimike
[Redakto | Redakto nëpërmjet kodit]Alkanet japin disa lloje reaksione si:
1- Reaksionë zëvendësimi, nga bashkëveprimi i halogjenëve aktivë siç janë bromi apo klori me alkanet në prani të dritës sjell zëvendësimin e hidrogjenit me halogjen, p.sh.:
CH3-CH2-CH3 + Br2 → CH3-CH2-CH2-Br2 + HBr
2-Reaksionë oksidimi, kontrolli i alkaneve çon në formimin e një sërë komponimesh si p.sh.:
CH4 → CH3OH (metanol) CH4 → CH2O (metanal)
