Tretësirat: Dallime mes rishikimesh
| [Redaktim i kontrolluar] | [Redaktim i kontrolluar] |
Smallem (diskuto | kontribute) v Përmirësime teknike dhe rregullime të gabimeve me referimet: (-(\{\{\s*cit[aeio][^\}]*\|\s*(?:access\-?|archive\-?|doi\-broken\-|lay\-|pmc\-embargo\-|publication\-|air\-?)?date\s*=\s*\d{1,2} +)April( +\d{4}) +\1prill\2) |
Nixfer (diskuto | kontribute) vNo edit summary |
||
| Rreshti 1: | Rreshti 1: | ||
[[ |
[[Skeda:SaltInWaterSolutionLiquid.jpg|parapamje|180px|Tretësira fiziologjike e NaCl, e cila formohet duke shtuar substancën e tretur (NaCl) në tretës (Uji)]] |
||
'''Tretësirat''' janë sisteme homogjene të përbëra nga dy ose më shumë komponentë. Nëse nga dy substanca është formuar një përzierje homogjene, një përzierje të tillë e quajmë tretësirë. |
'''Tretësirat''' janë sisteme homogjene të përbëra nga dy ose më shumë komponentë. Nëse nga dy substanca është formuar një përzierje homogjene, një përzierje të tillë e quajmë tretësirë. |
||
Tretësirat përbëhen prej dy komponentëve; tretësit dhe substancës së tretur. |
Tretësirat përbëhen prej dy komponentëve; tretësit dhe substancës së tretur. |
||
| Rreshti 8: | Rreshti 8: | ||
Tretësira ka gjendje agregate të njejtë me gjendjen agregate të tretësit. |
Tretësira ka gjendje agregate të njejtë me gjendjen agregate të tretësit. |
||
Procesi i lidhjes së molekulave të tretësit joujor (amoniakut të lëngët, metanolit , etanolit, flourhidrikut etj,) në jone të substancës së tretur quhet |
Procesi i lidhjes së molekulave të tretësit joujor (amoniakut të lëngët, metanolit , etanolit, flourhidrikut etj,) në jone të substancës së tretur quhet ''Solvatim''. Produktet e këtij procesi ''Solvate''. Në rastet ku si tretës përdoret uji procesi quhet ''Hidratim''. Produktet e këtij procesi quhen ''Hidrate''. |
||
Uji në disa hidrate mund të formojë kristalhidrate, si: <chem>FeSO4</chem> x <chem>7H2O</chem>, <chem>CuSO4*5H2O</chem> etj, kjo sasi e ujit e cila është pjesë përbërëse e strukturës së kristalit, quhet Uji Kristalor. |
Uji në disa hidrate mund të formojë kristalhidrate, si: <chem>FeSO4</chem> x <chem>7H2O</chem>, <chem>CuSO4*5H2O</chem> etj, kjo sasi e ujit e cila është pjesë përbërëse e strukturës së kristalit, quhet Uji Kristalor. |
||
Sipas gjendjes agregate tretësirat mund të ndahen në nëntë grupe kryesore. Më të rëndësishme janë: |
Sipas gjendjes agregate tretësirat mund të ndahen në nëntë grupe kryesore. Më të rëndësishme janë: |
||
| Rreshti 20: | Rreshti 18: | ||
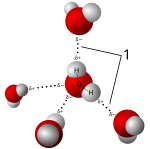
[[File:3D model hydrogen bonds in water.svg|left|thumb|150px|Modeli 3D i ujit si tretësi më i mirë dhe universal]] |
[[File:3D model hydrogen bonds in water.svg|left|thumb|150px|Modeli 3D i ujit si tretësi më i mirë dhe universal]] |
||
Tretësit klasifikohen në tretës polar (kryesisht janë komponime inorganike) dhe në tretës jopolar (kryesisht janë komponime organike) |
Tretësit klasifikohen në tretës polar (kryesisht janë komponime inorganike) dhe në tretës jopolar (kryesisht janë komponime organike) |
||
Nga [[Substanca|Substancat]] më të njohura të tretshme në ujë janë kryesisht; të gjiha [[nitrati|nitratet]] dhe acetatet, pastaj të gjitha [[Klori|Kloruret]], [[Bromi|Bromuret]] dhe [[Jodi|Joduret]], përvec halogjenureve të [[argjendi|argjendit]], halogjenureve [[ |
Nga [[Substanca|Substancat]] më të njohura të tretshme në ujë janë kryesisht; të gjiha [[nitrati|nitratet]] dhe acetatet, pastaj të gjitha [[Klori|Kloruret]], [[Bromi|Bromuret]] dhe [[Jodi|Joduret]], përvec halogjenureve të [[argjendi|argjendit]], halogjenureve [[Zhiva|merkurore]] dhe halogjenureve të [[Plumbi]]t. [[Sulfat]]et e patretshme janë: <chem>BaSO4, SrSO4, PbSO4</chem>, ndërsa <chem>Ag2SO4</chem>, tretet pak në ujë. |
||
| ⚫ | |||
| ⚫ | |||
Duke u bazuar në madhësinë e grimcave që formojnë tretësirën, tretësirat ndahen në: |
Duke u bazuar në madhësinë e grimcave që formojnë tretësirën, tretësirat ndahen në: |
||
* Tretësira të vërteta, të cilat përbëhen prej grimcave që kanë diametër afro 1nm |
* Tretësira të vërteta, të cilat përbëhen prej grimcave që kanë diametër afro 1nm |
||
| Rreshti 36: | Rreshti 32: | ||
* Suspensionet janë përzierje heterogjene me grimca të pezulluara, të cilat pas një kohe fundërrojnë, këto tretësira përbëhen prej grimcave me diametër mbi 100nm. |
* Suspensionet janë përzierje heterogjene me grimca të pezulluara, të cilat pas një kohe fundërrojnë, këto tretësira përbëhen prej grimcave me diametër mbi 100nm. |
||
Varësisht nga sasia e substancës së tretur dhe tretësit, ekzistojnë tri lloje të tretësirave: |
Varësisht nga sasia e substancës së tretur dhe tretësit, ekzistojnë tri lloje të tretësirave: |
||
| Rreshti 43: | Rreshti 38: | ||
* Të tejngopura, kur përmban më tepër sustancë të tretur sesa tretësira e ngopur. Kjo tretësirë është jo stabile, sepse nën ndikimin e kushteve të jashmte (tundja) menjëherë shndrrohet në tretësirë të ngopur, sepse teprica e substancës së tretur ndahet në formë të kristaleve. Shumë substanca mund të formojnë tretësira të tejngopura, si: <chem>CuSO4*5H2O, Na2SO4*10H2O, Na2SO3*5H20</chem> |
* Të tejngopura, kur përmban më tepër sustancë të tretur sesa tretësira e ngopur. Kjo tretësirë është jo stabile, sepse nën ndikimin e kushteve të jashmte (tundja) menjëherë shndrrohet në tretësirë të ngopur, sepse teprica e substancës së tretur ndahet në formë të kristaleve. Shumë substanca mund të formojnë tretësira të tejngopura, si: <chem>CuSO4*5H2O, Na2SO4*10H2O, Na2SO3*5H20</chem> |
||
==Referimet== |
== Referimet == |
||
{{reflist}} |
{{reflist}} |
||
[[Kategoria:Kimi]] |
[[Kategoria:Kimi]] |
||
Versioni i datës 21 mars 2022 21:47

Tretësirat janë sisteme homogjene të përbëra nga dy ose më shumë komponentë. Nëse nga dy substanca është formuar një përzierje homogjene, një përzierje të tillë e quajmë tretësirë. Tretësirat përbëhen prej dy komponentëve; tretësit dhe substancës së tretur. [1] Tretësi është komponentë e cila gjendet në sasi më të madhe, ndërsa substanca e tretur është komponentë me sasi më të vogël në tretësirë.
Substanca e tretur (B) + Tretësi (A) = Tretësira (T)
Tretësira ka gjendje agregate të njejtë me gjendjen agregate të tretësit. Procesi i lidhjes së molekulave të tretësit joujor (amoniakut të lëngët, metanolit , etanolit, flourhidrikut etj,) në jone të substancës së tretur quhet Solvatim. Produktet e këtij procesi Solvate. Në rastet ku si tretës përdoret uji procesi quhet Hidratim. Produktet e këtij procesi quhen Hidrate. Uji në disa hidrate mund të formojë kristalhidrate, si: x , etj, kjo sasi e ujit e cila është pjesë përbërëse e strukturës së kristalit, quhet Uji Kristalor.
Sipas gjendjes agregate tretësirat mund të ndahen në nëntë grupe kryesore. Më të rëndësishme janë:
- tretësirë e lëngët (ujë-alkool, ujë-sheqer)
- e ngurtë, Aliazhet (Ar- Bakër)
Tretësi më i mirë dhe më universal i substancave kimike është uji. Uji si molekulë polare ka aftësi të mëdha për të tretur substanca të ndryshme, mirëpo uji nuk ka aftësi për tretjen e shumë substancave organike, sepse ato janë jopolare. Për tretjen e këtyre substancave jopolare përdoren tretës jopolarë, si : eteri, kloroformi, benzeni etj.
Tretësit klasifikohen në tretës polar (kryesisht janë komponime inorganike) dhe në tretës jopolar (kryesisht janë komponime organike) Nga Substancat më të njohura të tretshme në ujë janë kryesisht; të gjiha nitratet dhe acetatet, pastaj të gjitha Kloruret, Bromuret dhe Joduret, përvec halogjenureve të argjendit, halogjenureve merkurore dhe halogjenureve të Plumbit. Sulfatet e patretshme janë: , ndërsa , tretet pak në ujë.
Ndarja e tretësirave
Duke u bazuar në madhësinë e grimcave që formojnë tretësirën, tretësirat ndahen në:
- Tretësira të vërteta, të cilat përbëhen prej grimcave që kanë diametër afro 1nm
- Tretësira koloidale, të cilat janë të përbëra prej grimcave me madhësi prej 1 deri 100 nm
Lëngjet dhe substancat e ngurta të tretura në gaze quhen Aerosole, si psh: Deodorantët, Mjegulla, Tymi
Emulzionet janë koloide në të cilat lëngjet janë të tretura në lëngje tjera apo substanca të ngurta, si: Majonezi, Djathi
Solet janë koloide kur substanca e ngutë tretet në lëngje apo substanca tjera të ngurta, si: Gelli, Ngjyrat
- Suspensionet janë përzierje heterogjene me grimca të pezulluara, të cilat pas një kohe fundërrojnë, këto tretësira përbëhen prej grimcave me diametër mbi 100nm.
Varësisht nga sasia e substancës së tretur dhe tretësit, ekzistojnë tri lloje të tretësirave:
- Të pangopura, atëherë kur tretësi mund të tretë sasi të reja të substancës së tretur
- Të ngopura, kur në një temperaturë të caktuar, tretësi nuk mund të tret më substancë
- Të tejngopura, kur përmban më tepër sustancë të tretur sesa tretësira e ngopur. Kjo tretësirë është jo stabile, sepse nën ndikimin e kushteve të jashmte (tundja) menjëherë shndrrohet në tretësirë të ngopur, sepse teprica e substancës së tretur ndahet në formë të kristaleve. Shumë substanca mund të formojnë tretësira të tejngopura, si:
Referimet
- ^ "Solutions". Washington University Chemistry Department. Washington University. Marrë më 13 prill 2018.
{{cite web}}: Mungon ose është bosh parametri|language=(Ndihmë!)






